Para muchas parejas que tratan de concebir sin éxito, hay una serie de tratamientos de fertilidad avanzados conocidos como Tecnologías de Reproducción Asistida.
Fertilización in vitro (IVF)
Se administran inyecciones de hormonas para estimular la producción y liberación de óvulos. Se unen los óvulos y los espermatozoides en una placa de laboratorio, lo que explica el nombre del proceso in vitro. In Vitro en latín significa en el vidrio. Si se logra fertilizar algún ovocito, se transferirá un número predeterminado de embriones al útero de la mujer. Si tiene suerte, uno de ellos logrará implantarse y comenzará a desarrollarse.
Generalmente se pueden describir cinco etapas de la IVF:
 |
| Fertilización in vitro (IVF) |
Paso uno: Estimulación ováricaLa meta es ayudar a varios ovocitos a que maduren, estimulando los ovarios con hormonas que se inyectan durante varios días. Esto resulta necesario porque no se fertilizan todos los ovocitos y no se desarrollan todos los embriones o implantes que se hacen en el útero. Las ecografías y los exámenes de sangre permiten al médico observar el número y tamaño de folículos que están madurando, así como el espesor del revestimiento uterino. Cuando el monitoreo ecográfico indica que los ovocitos dentro del folículo están por madurar, se inyecta otra hormona para inducir la maduración final del folículo y la ovulación.
Paso dos: Recuperación de ovocitos
Los ovocitos deben ser recuperados dentro de las 36 a 38 horas de la inducción de la maduración del folículo. De no ser así, los ovocitos desaparecerán y se harán inaccesibles para completar el tratamiento. La recuperación de ovocitos habitualmente se realiza por vía vaginal bajo guía ecográfica, utilizando una aguja larga hueca.
Paso tres: Fertilización
El mismo día de la recuperación de ovocitos, se brinda una muestra fresca de semen obtenida por masturbación y refinada en el laboratorio para optimizar las capacidades de los espermatozoides. Se unen entonces los ovocitos y los espermatozoides en una placa de Petri (o con el procedimiento ICSI) y se cultivan en una incubadora durante 24 horas. Si ocurre la fusión, se dejan madurar los huevos fertilizados otros 2-3 días para transferencia de embriones, o 5-6 días para transferencia de blastocito.
Se vuelve a transferir uno o más embriones nuevamente al útero utilizando un cateter fino y blando adosado a una jeringa roma cargada con un embrión o embriones. El procedimiento realizado en la clínica es relativamente simple e indoloro.
Paso cinco: Apoyo a la fase lútea
Luego de la transferencia de embriones se le da hormonas a la mujer, que el cuerpo normalmente produce durante la segunda mitad del ciclo menstrual. Esto engrosa el revestimiento del útero para prepararlo para aceptar la implantación de un huevo fertilizado.
Hasta 30% de los pacientes sometidos a estimulación ovárica tienen un caso leve de síndrome de hiperestimulación ovárica (SHEO)1. En el SHEO moderado, las pacientes pueden desarrollar o acumular líquido dentro de la cavidad abdominal, presentar dolores abdominales, náuseas y síntomas gastrointestinales. Si usted presenta estos síntomas infórmeselo a su médico inmediatamente. Habitualmente el SHEO leve puede ser manejado con analgésicos de venta libre y una reducción de la actividad1. La sobrestimulación severa puede requerir internación. Sin embargo, el monitoreo regular reduce el riesgo de efectos colaterales a un 2%1 o menos. |
Este procedimiento de laboratorio a menudo es utilizado en conjunto con la fertilización in vitro si el varón tiene un recuento bajo de espermatozoides, baja motilidad de los espermatozoides, o mala calidad del esperma. Utilizando una guía microscópica, un técnico de laboratorio inyecta un único espermatozoide directamente dentro de un ovocito. Si ocurre la fusión, el embrión se transfiere en el útero para su implantación.
Otros tratamientos
Transferencia Intratubárica de Gametos (GIFT)
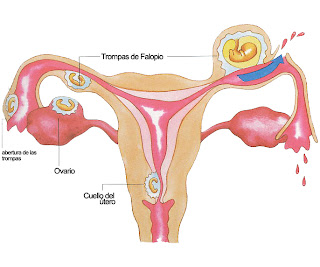
Este tratamiento permite los mismos procedimientos que IVF excepto que la fertilización ocurre en el interior del cuerpo (in vivo, dentro de las trompas de Falopio). El GIFT sólo se puede realizar si las trompas de Falopio están sanas.
La fertilización no puede verificarse inmediatamente dado que GIFT tiene lugar in vivo. |
Transferencia Intratubárica de Cigotos (ZIFT)
Este tratamiento sigue los mismos procedimientos que IVF excepto que los huevos fertilizados se colocan en la trompa de Falopio en una etapa específica más temprana del desarrollo del embrión.
ZIFT solo se puede realizar si las trompas de Falopio están indemnes.
|
Extracción de Espermatozoides de los Testículos (TESE) y Aspirado Microquirúrgico de Espermatozoides del Epidídimo (MESA)
 |
| Extracción de espermatozoides del testículo |
En algunos casos, por ejemplo cuando hay un bloqueo de los canales espermáticos, no hay ningún espermatozoide en la eyaculación. Aún así, tal vez sea posible obtener espermatozoides directamente de los testículos (TESE) o del Epidídimo (MESA). Se realiza un procedimiento quirúrgico menor para extraer muestras de tejido, que pueden contener espermatozoides. Estos procedimientos requieren anestesia local y habitualmente no son dolorosos. Los espermatozoides se usan luego en el tratamiento ICSI.
Habitualmente en un procedimiento se pueden recuperar suficientes espermatozoides para congelar y utilizar más adelante de ser necesario.
|
Eclosión asistida
Antes de implantar en el útero, el embrión debe salir de su cobertura en un proceso denominado eclosión. En algunas mujeres la membrana parece endurecerse con la edad, interfiriendo con el proceso de eclosión.
En esos casos, la perforación de la membrana del embrión con una solución ácida diluida o con láser antes de la transferencia de embriones puede ayudar en la eclosión. Este procedimiento se realiza en embriones en el laboratorio cuando es necesario. Las mujeres de más edad o aquellas que no han alcanzado el embarazo después de varios ciclos de IVF a menudo pueden beneficiarse con este tratamiento.
 |
| Congelamiento de embriones |
Congelado de huevos y embriones
La criopreservación, conocida también como congelado, consiste en almacenar huevos o embriones a una temperatura muy baja para poderlos utilizar más adelante. Permite hacer un ciclo de tratamiento en el futuro sin tener que repetir el proceso de estimulación hormonal y recuperación de los ovocitos.
El riesgo de tener un embarazo múltiple al someterse a un tratamiento de infertiliadad es mayor que el habitual, pero se puede minimizar. Actualmente, de los embarazos conseguidos con IVF e ICSÍ, como promedio 21% son gemelares y 1% son trillizos2. Esto es fundamentalmente debido a la práctica de transferir los embriones al útero para aumentar las probabilidades de éxito. Analice con su médico maneras de minimizar el riesgo de gestaciones múltiples.
Donación de óvulos
La donación de óvulos consiste en que otra mujer donde sus óvulos para que la receptora que es incapaz de utilizar los óvulos propios pueda concebir. En la donación de óvulos se realiza IVF de la manera habitual, excepto que la donante recibe medicación para estimular la producción de óvulos. Al mismo tiempo, la receptora también recibe medicación para que su ciclo imite el de la donante y que su cuerpo esté preparado para recibir al embrión. Luego se fertilizan los óvulos en un laboratorio utilizando el espermatozoide de la pareja de la receptora y se transfieren los embriones al útero de la receptora.
Diagnóstico Genético Pre Implantación (DGP)
El DGP es una técnica que se puede utilizar en el contexto de una IVF para analizar los embriones, buscando una serie de trastornos genéticos. Las pruebas se hacen en el laboratorio antes de transferir el embrión al útero. Esto disminuye el riesgo de tener un hijo con una enfermedad hereditaria grave. Se puede hacer un screening para detectar una serie de trastornos, incluyendo síndrome de Down, fibrosis quística, hemofilia A, enfermedad de Tay-Sachs, y síndrome de Turner. El DGP está indicado solo en algunas afecciones bien definidas.
No existe una tasa de éxitos absolutos de los tratamientos de fertilidad y los promedios pueden ser engañosos. Depende de muchos factores, incluyendo su edad, la causa de sus dificultades para concebir y la pericia de los médicos. |
REFERENCIAS